- Küldje el az oldalt ismerősének!
-
-
facebook
-
google +
-
Nyomtatóbarát változat
-
Az oldal elküldése e-mailben
Egészség–EU Hírlevél
166 -
Fókuszban
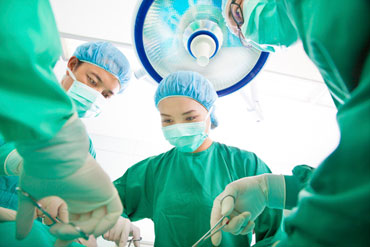
Mennyire biztonságos az uroginekológiai műtétek során használt sebészeti háló?
szerző: dr. Christopher Chapple, az Európai Urológus Társaság főtitkára és az ÚÚAKTB sebészeti hálókról szóló véleményének előadója

Mivel uroginekológiai műtéteknél egyre gyakrabban használnak sebészeti hálót, az ennek kapcsán fellépő káros hatásokról – fertőzésről, szövetpusztulásról, a háló kilökődéséről vagy zsugorodásáról, illetve fájdalomról és szexuális diszfunkcióról – is egyre több beszámoló érkezik. Az Európai Bizottság ezért felkérte az új és újonnan azonosított egészségügyi kockázatok tudományos bizottságát (ÚÚAKTB), hogy mérje fel a sebészeti háló használatának egészségügyi kockázatait.
A felkérésnek eleget téve az ÚÚAKTB megvizsgálta a medencefenék működészavarának kezelési lehetőségeit. A vizsgálat során áttekintette a témakörrel kapcsolatos legfrissebb szakirodalmat, a tudományos társaságok és egészségügyi hatóságok iránymutatásait, a sebészeti és a nem sebészeti kezelési módszereket, valamint a különböző hálófajták leírásait. A vizsgálat alapján született vélemény elsődlegesen az uroginekológiai műtétekhez használt hálók egészségügyi kockázataival foglalkozik, és kitér arra, miként lehet meghatározni a fokozottan veszélyeztetett betegcsoportokat, és mely területeken érdemes értékeléseket végezni.
Az ÚÚAKTB megállapította, hogy a hálóbeültetés klinikai kimenetelét számos tényező befolyásolja, így az anyag tulajdonságai, a termék kialakítása, a hálóméret, a beültetés módja, a beteg adottságai, a kapcsolódó eljárások (pl. a méh eltávolítása) vagy a sebész jártassága. A megfelelő kezeléshez pedig e tényezők mindegyikét figyelembe kell venni.
A szintetikus hálók egészségügyi kockázatainak felmérésekor egyértelmű különbséget kell tenni a stressz-inkontinencia kezelésére alkalmazott hüvelyiszalag-műtéttel járó kisebb kockázatok, illetve a kismedencei szervek süllyedésének kezelésére alkalmazott hálóbeültető műtét kockázatai között.
A véleményben megfogalmazott megállapításai alapján az ÚÚAKTB a stressz-inkontinencia kezelésére alkalmazott hüvelyiszalag-műtétek esetében pozitívan nyilatkozik a szintetikus háló további használatáról, mivel ez az elfogadott eljárás – ha gyakorlott és megfelelően képzett sebész végzi – a legtöbb mérsékelten súlyos vagy súlyos stressz-inkontinenciával kezelt beteg esetében bizonyítottan hatásos és biztonságos.
Az ÚÚAKTB ugyanakkor a szintetikus háló vaginán keresztüli alkalmazását a női kismedencei szervek süllyedése miatt szükségessé váló helyreállító műtétekhez nem támogatja. Mivel egy ilyen beavatkozás fokozott kockázattal jár, kizárólag akkor célszerű végrehajtani, ha más sebészeti eljárások nem jártak, vagy feltehetőleg nem járnának sikerrel.
A feltárt kockázatok értékelése alapján a szintetikus hálók közül vaginán keresztüli alkalmazásra az 1. típusú polipropilén háló, hasi úton történő behelyezésre pedig az 1. típusú polipropilén és a 3. típusú poliészter háló a legmegfelelőbb.
Az optimális eredmény eléréséhez a sebészeti beavatkozásoknál általában – de különösen az említett műtéteknél – kiemelten fontos a betegek megfelelő kiválasztása és a betegtanácsadás.
Az ÚÚAKTB azt ajánlja, hogy lehetőség szerint a sebész egy-egy beavatkozáshoz a lehető legkevesebb hálót használja fel. A bizottság további javaslata, hogy a jelenlegi nemzetközi iránymutatások alapján és az érintett európai sebészeti társaságokkal közösen a szakma dolgozzon ki egy képesítési rendszert a sebészek számára.
A teljes értékelés és a sebészeti háló uroginekológiai műtétek során történő használatának további részletei a 2015 decemberében közzétett, és az előzetes véleményről szóló nyilvános konzultáció nyomán készült végleges véleményben olvashatók. A kérdést közérthetően áttekintő tájékoztató már ugyancsak elérhető.
http://ec.europa.eu/dgs/health_food-safety/dyna/enews/enews.cfm?al_id=1656
Harmadik végleges vélemény a szintetikus biológiáról: A szintetikus biológia környezeti és a biodiverzitást fenyegető veszélyei, valamint a szintetikus biológiai kutatás prioritásai.
Az Európai Bizottság és nem élelmiszer jellegű termékekkel foglalkozó tudományos bizottságai 2015 decemberében közzétették a szintetikus biológiáról szóló harmadik és egyben utolsó tudományos szakvéleményüket „A szintetikus biológia környezeti és a biodiverzitást fenyegető veszélyei, valamint a szintetikus biológiai kutatás prioritásai” címmel.
Az első vélemény a szintetikus biológia alkalmazási körét, fogalmának meghatározását, valamint a szintetikus biológia és a géntechnológia hasonlóságait és különbségeit ismertette. Az ENSZ szintetikus biológiával foglalkozó eseti szakértői munkacsoportja – elismerve a három tudományos bizottság, azaz az ÚÚAKTB, az EKKTB és az FBTB munkáját, valamint az általuk kidolgozott ajánlások nemzetközileg is kiemelkedő tudományos színvonalát – a közelmúltban jóváhagyta a szintetikus biológia fogalmának meghatározását. Eszerint „a szintetikus biológia a természettudományok, a technológia és a műszaki tudományok alkalmazása genetikai anyagok élő szervezetekben való tervezésének, előállításának, és/vagy módosításának lehetővé tétele és felgyorsítása érdekében”.
A második vélemény két kérdést vizsgált meg közelebbről: egyfelől azt, hogy a szintetikus biológia terén várható fejlemények előreláthatólag milyen hatást gyakorolnak az emberekre, az állatokra és a környezetre, másfelől pedig azt, hogy a géntechnológiával módosított szervezetek egészségügyi és környezeti kockázatértékelésére szolgáló uniós módszerek vajon a szintetikus biológia esetében is alkalmazhatók-e. A tudományos bizottságok emellett felkérést kaptak arra, hogy újabb, átdolgozott kockázatértékelési módszereket és kockázatcsökkentési eljárásokat javasoljanak, többek között az úgynevezett biztonsági zárak alkalmazása tekintetében.
A nemrég közzétett harmadik vélemény pedig nemcsak azokat a jelentős tudásbeli hiányosságokat veszi sorra, amelyeket a kockázatok megbízható felmérésénél figyelembe kell venni, de e hiányosságok alapján kutatási ajánlásokat is megfogalmaz.
A tudományos bizottságok elemzésükben kizárólag a közeljövő várható fejleményeivel foglalkoznak, utalva arra, hogy megállapításaikat néhány év múlva – a szintetikus biológiai technológia fejlődésének tükrében – érdemes lesz felülvizsgálni és aktualizálni.
Kapcsolódó hír, hogy 2015. december 10-én, a Luxemburgi Egyetem belvali campusán az Európai Bizottság a luxemburgi elnökség égisze alatt műhelytalálkozót tartott a szintetikus biológiáról. Az eseményen az Európai Bizottságnak alkalma nyílt arra, hogy a megjelent tudósok, kockázatértékelési szakemberek, kockázatkezelők, politikai döntéshozók és a tudományos közösség képviselői körében ismertesse a szintetikus biológia témakörében született véleményeket, illetve a területen végzett egyéb tevékenységeit. A résztvevők ezenkívül különböző nézőpontokból is megvizsgálhatták a szintetikus biológia témakörét, és megoszthatták egymással álláspontjaikat és tapasztalataikat.
http://ec.europa.eu/dgs/health_food-safety/dyna/enews/enews.cfm?al_id=1655
Az FBTB kozmetikai összetevők vizsgálatához és biztonsági értékeléséhez készített útmutató jegyzeteinek legfrissebb kiadása
A fogyasztók biztonságával foglalkozó tudományos bizottság (FBTB) tagjai által kidolgozott útmutató jegyzet célja, hogy összefoglalja a kozmetikai anyagok európai vizsgálatának és biztonsági értékelésének különböző szempontjaival kapcsolatos tudnivalókat. A dokumentum elsősorban a kozmetikai termékek összetevőivel foglalkozik és iránymutatást nyújt a késztermékek biztonsági értékeléséhez, de a hatóságok és a kozmetikai ipar számára is hasznos lehet a kozmetikai termékekre vonatkozó hatályos uniós jogszabályok érvényre juttatásához, illetve betartásához. Noha a jegyzet mindenekelőtt a termékösszetevőkkel, és nem a késztermékekkel foglalkozik, az abban olvasható tudnivalók a kozmetikai késztermékek uniós jogban előírt termékinformációs dokumentációjának összeállításához is jól hasznosíthatók.
Az útmutató jegyzeteket az FBTB rendszeresen frissíti. A mostani aktualizálás előzménye, hogy a legutóbbi, 2012-es kiadás óta a dokumentum több ponton is kiegészült, a tartalmával kapcsolatban pedig számos érdemi vélemény és feljegyzés született. További fejlemény, hogy 2013-ban módosult a kozmetikai termékek uniós szabályozása. Ennek értelmében immár minden olyan késztermék forgalmazása tilos, amely 2013 utáni állatkísérletekkel tesztelt összetevőket vagy ilyen összetevők kombinációját tartalmazza.
A kozmetikai termékekről szóló rendelet értelmében a piaci forgalomba hozott kozmetikai termékeknek – rendeltetésszerű használattal és reálisan előrelátható felhasználási feltételekkel számolva – biztonságosaknak kell lenniük az emberi egészségre nézve. A kozmetikai termékek a gyakorlatban csak nagyon ritkán bizonyulnak súlyosan ártalmasnak az egészségre, ez azonban nem jelenti azt, hogy használatuk eleve biztonságos. Főleg a hosszú távú biztonságosságra kell odafigyelnünk, mivel kozmetikai termékeket esetenként szinte egész életünkben használunk.
A különös aggodalomra okot adó anyagok (pl. a színezékek, a tartósítószerek és UV-szűrők) biztonsági értékelését az Európai Bizottság megbízásából az FBTB végzi. A vizsgálat során az FBTB a rendelkezésre álló tudományos, illetve klinikai adatokat, a vonatkozó epidemiológiai tanulmányokat, a baleseti információkat és a humán vonatkozású adatokat egyaránt áttekinti.
Az útmutató jegyzet 2015. évi aktualizált, kilencedik kiadásában az FBTB külön fejezetben tárgyalja azokat az állatkísérleteket helyettesítő megoldásokat, amelyek a kozmetikai anyagok biztonságának vizsgálatához használhatóak. A kozmetikai termékekről szóló új rendeletben bevezetett és az útmutató jegyzetek e legfrissebb kiadásában is szereplő legfontosabb változások közé tartoznak még a következők: a kozmetikai termékekre vonatkozó biztonsági követelmények szigorítása, a felelős személy fogalmának bevezetése, az Európai Unióban forgalomba hozott kozmetikai termékek központosított bejelentése, a súlyos nemkívánatos hatások bejelentésének bevezetése, a nanoanyagok kozmetikai termékekben való használatának új szabályai, valamint a rákkeltő, mutagén vagy reprodukciót károsító anyagokra vonatkozó követelmények bevezetése.
A dokumentum nem egyfajta ellenőrző lista, az abban megfogalmazott intézkedések eseti alapon alkalmazandók. Ezt egyébként az FBTB is hangsúlyozza, kiemelve, hogy a kozmetikai anyagok és a késztermékek biztonsági értékelése kizárólag eseti alapon történhet.
http://ec.europa.eu/health/scientific_committees/consumer_safety/docs/sccs_o_190.pdf
Előzetes vélemény a gyermekek szervezetébe jutó játékanyagok becsült mennyiségéről
Az Európai Bizottság felkérte az egészségügyi és környezeti kockázatok tudományos bizottságát (EKKTB) annak vizsgálatára, hogy három különböző játékanyag gyermekek szervezetébe való jutásával kapcsolatban jelenleg rendelkezésre álló adatok fényében továbbra is megfelelőek-e a hatályos kioldódási határértékek. Az elsődleges kérdés az volt, hogy a száraz, törékeny, porszerű vagy hajlékony játékanyagok szervezetbe jutására vonatkozó 100 milligrammos, illetve a folyékony vagy ragacsos állagú játékanyagok szervezetbe jutására vonatkozó 400 milligrammos maximális napi határérték felváltható-e heti határértékkel.
Az EKKTB áttanulmányozta az e témában 2008 óta megjelent szakirodalmat, majd előzetes véleményt készített, amelyben megállapítja, hogy a hatályos kioldódási határértékek helytállóak, és a szervezetbe jutásra vonatkozó határértékeket továbbra is napi alapon kell meghatározni.
Az előzetes vélemény már az interneten is elérhető, és 2016. február 14-ig nyilvános konzultáció keretében véleményezhető.
http://ec.europa.eu/dgs/health_food-safety/dyna/enews/enews.cfm?al_id=1657