- Изпратете на приятел
-
-
facebook
-
google +
-
Версия за печат
-
E-mail this page
Здраве-ЕС - електронен бюлетин
166 -
В центъра на вниманието
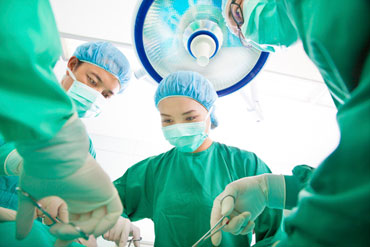
Безопасно ли е използването на хирургически мрежи в урогинекологичната хирургия?
от професор д-р Кристофър Чапъл, генерален секретар на Европейската асоциация по урология и докладчик по становището на Научния комитет по възникващи и идентифицирани нови здравни рискове (НКВИНЗР) относно хирургичес

Поради все по-честото използване на хирургически мрежи в урогинекологичната хирургия зачестиха случаите на неблагоприятно въздействие, свързано с тяхната употреба, като например инфекции, ерозия на тъкани, експозиция или свиване на мрежата, болки и сексуална дисфункция. Ето защо Европейската комисия поиска от своя независим Научен комитет по възникващи и идентифицирани нови здравни рискове (НКВИНЗР) да проучи рисковете за здравето, свързани с използването на хирургически мрежи.
НКВИНЗР разгледа различните възможности за лечение на дисфункция на тазовото дъно, като консултира актуални научни публикации и насоки от научни дружества и здравни органи, обръщайки внимание едновременно на нехирургическите и хирургическите методи за лечение и на различните видове мрежи. Изготвеното становище разглежда здравните рискове от различните мрежи, използвани в урогинекологичната хирургия, начините за определяне на високорисковите групи пациенти и нуждите при извършване на оценка.
НКВИНЗР установи, че клиничните резултати след имплантирането на мрежа зависят от редица фактори, сред които свойствата на материалите, формата на продукта, общия размер на мрежата, начина на имплантиране, характеристиките на пациента, свързаните процедури (напр. хистеректомия) и опита на хирурга. Всички те следва да се вземат предвид при избора на подходяща терапия.
При оценката на рисковете за здравето от синтетични мрежи е необходимо ясно да се направи разграничение между по-малките рискове, свързани с оперативното поставяне на слинг при стресова уринарна инконтиненция (СУИ), и тези, свързани с хирургична интервенция при пролапс на тазовите органи.
Въз основа на своите констатации НКВИНЗР подкрепя използването и занапред на синтетични слингове при оперативното лечение на СУИ, тъй като това е приета процедура с доказана ефикасност и безопасност при повечето пациенти с умерена до тежка СУИ, когато се практикува от опитен хирург с необходимата квалификация.
НКВИНЗР обаче не насърчава използването на синтетична мрежа при лечението на пролабирали женски тазови органи по влагалищен път. Поради високите рискове, свързани с този вид операция, тя следва да се извършва само когато други хирургични процедури не дадат резултат или се очаква да не са успешни.
Оценката на посочените рискове показва, че полипропиленовите мрежи от тип 1 са най-подходящите синтетични мрежи за вагинална употреба, а полипропиленовите от тип 1 и полиестерните от тип 3 — за въвеждане по коремен път.
Подходящият избор процедура за съответния пациент и консултациите са от изключително значение за постигането на оптимални резултати от всички хирургични процедури, особено тези от такова естество.
НКВИНЗР препоръчва използването на по-малка мрежа за всички процедури, когато това е възможно, и въвеждане на система за сертифициране на хирурзите, която ще се базира на съществуващите международни насоки и ще бъде създадена в сътрудничество със съответните европейски асоциации на хирурзите.
За пълната оценка и повече подробности относно използването на хирургически мрежи в урогинекологичната хирургия, моля, вижте окончателното становище, което бе публикувано през декември 2015 г. след обществена консултация относно предварителното становище. Можете да прочетете също информационен документ, съдържащ изготвен на достъпен език преглед по този въпрос.
http://ec.europa.eu/dgs/health_food-safety/dyna/enews/enews.cfm?al_id=1656
Окончателно становище относно синтетичната биология III: рискове за околната среда и биологичното разнообразие и приоритети за научни изследвания
През декември 2015 г. Европейската комисия и нейните научни комитети публикуваха окончателното си Становище относно синтетичната биология III: рискове за околната среда и биологичното разнообразие, свързани със синтетичната биология, и приоритети на научноизследователската дейност в областта на синтетичната биология, което е последното от три научни становища относно синтетичната биология (SynBio).
Първото становище бе насочено към обхвата и определението на синтетичната биология и доколко тя прилича на генното инженерство и се различава от него. Потвърждавайки международния престиж на научните комитети и научната издържаност на техните препоръки, специалната техническа експертна група на ООН по синтетична биология неотдавна прие определението на научните комитети за синтетичната биология, като „използване на науката, технологиите и инженерството за улесняване и ускоряване на проектирането, производството и/или модифицирането на генетични материали в живи организми“.
Второто становище бе насочено към последиците от вероятното развитие в областта на синтетичната биология за хората, животните и околната среда, както и към определянето на това дали съществуващите практики на Европейския съюз за оценка на риска за здравето и околната среда по отношение на генетично модифицирани организми са подходящи за синтетичната биология. Освен това от научните комитети бе поискано да направят предложения за преработени методи за оценка на риска и процедури за намаляване на риска, включително мерки за сигурност.
Публикуваното неотдавна трето становище посочва основните пропуски в познанията, които следва да се вземат предвид при извършването на надеждни оценки на риска, и предоставя препоръки за научни изследвания въз основа на установените пропуски в познанията.
Научните комитети ограничиха обхвата на своя анализ до обозримото бъдеще, като признават, че констатациите следва да бъдат преразгледани и актуализирани отново след няколко години в зависимост от развитието на технологиите в областта на синтетичната биология.
Също по темата, на 10 декември 2015 г. в Люксембургския университет в Белвал се проведе семинар, посветен на синтетичната биология, организиран от Европейската комисия и под егидата на люксембургското председателство. В семинара участваха учени, специалисти по оценка и управление на риска, създатели на политики и представители на академичните среди, а за Европейската комисия това бе възможност да представи становищата си относно синтетичната биология и да обсъди другите си дейности в тази област. Семинарът бе също така възможност за всички участници да разгледат синтетичната биология от различен ъгъл и да споделят своите виждания и опит.
http://ec.europa.eu/dgs/health_food-safety/dyna/enews/enews.cfm?al_id=1655
Преработени указания на НКБП за изпитване на козметичните съставки и за оценка за тяхната безопасност
Указанията представляват документ, изготвен от членовете на Научния комитет по безопасност на потребителите (НКБП), в който се съдържа информация относно различните аспекти на изпитването и оценката на безопасността на козметичните вещества в Европа. Акцентът е върху козметичните съставки, въпреки че някои указания се отнасят и за извършването на оценка на безопасността на крайни продукти. Указанията имат за цел да помогнат на публичните органи и на козметичната индустрия да изпълнят разпоредбите на настоящото законодателство на ЕС за козметичните продукти. Въпреки че се отнасят главно за съставки, а не за крайни продукти, указанията наистина могат да бъдат от полза при съставянето на досието с информация за готов козметичен продукт, което се изисква понастоящем по силата на европейското право.
Указанията се актуализират редовно. След последното им преработване през 2012 г. бяха приети нови допълнения, становища и меморандуми от значение за съдържанието на указанията, което наложи последната актуализация. Освен това от 2013 г. насам европейското законодателство за козметичните продукти беше изменено и понастоящем забранява пускането на пазара на готови продукти, съдържащи съставки или комбинации от съставки, които са били изпитвани с използването на животни след 2013 г.
В Регламента относно козметичните продукти се посочва, че даден козметичен продукт, предлаган на пазара, е безопасен за човешкото здраве, когато се използва при нормални или разумно предвидими условия на употреба. На практика, козметичните продукти рядко са свързвани със сериозни опасности за здравето, но това не означава, че козметичните продукти като такива са безопасни за употреба. Нужно е да се обърне специално внимание на дългосрочната безопасност, тъй като козметичните продукти могат да се използват през по-голямата част от живота на човека.
За вещества като оцветители, консерванти и UV-филтри, които предизвикват особена загриженост, оценката на безопасността се извършва на ниво Комисия от НКБП, като се разглеждат всички налични научни и клинични данни, епидемиологични изследвания, информация, свързана със злополуки, и всякакви други подходящи данни по отношение на хората.
В актуализираната версия от 2015 г., която представлява 9-тото преработване на този документ, НКБП обърна специално внимание на алтернативите на изпитванията върху животни, които са подходящи за изпитвания на безопасността на козметичните съставки. Сред другите най-значителни промени, въведени от новия Регламент за козметичните продукти и отразени при настоящото преработване, са по-строгите изисквания за безопасност за козметичните продукти, въвеждането на понятието „отговорно лице“, централизираният подход за нотифициране за всички козметични продукти на пазара на ЕС, въвеждането на докладване за сериозни нежелани ефекти (СНЕ), новите правила за употребата на наноматериали в козметичните продукти, както и въвеждането на набор от изисквания за канцерогенните, мутагенните или токсичните за репродукцията (CMR) вещества.
Указанията не представляват контролен списък, а имат за цел да бъдат използвани поотделно за всеки отделен случай. В действителност НКБП подчертава, че оценката на безопасността на козметичните съставки и готовите продукти може да се извършва индивидуално във всеки отделен случай.
http://ec.europa.eu/health/scientific_committees/consumer_safety/docs/sccs_o_190.pdf
Предварително становище относно оценката на количеството материали от детски играчки, поглъщани от деца
Научният комитет по рисковете за здравето и околната среда (НКРЗОС) беше призован да направи преглед на съществуващите данни относно поглъщането от деца на три вида материали за играчки, за да се прецени дали настоящите гранични стойности на миграция все още са подходящи. Поставен бе въпросът дали дневните граници на поглъщане в размер на 100 mg за сух, трошлив, прахообразен или гъвкав материал от играчката и 400 mg за течен или лепкав материал от играчката могат да бъдат превърнати в седмични ограничения.
НКРЗОС извърши преглед на съответните публикации от 2008 г. насам, след което изготви предварително становище, според което настоящите гранични стойности на миграция са подходящи и всички граници на поглъщане следва да останат класирани като дневни, а не като седмични.
Предварителното становище вече е достъпно онлайн и ще бъде предмет на обществена консултация до 14 февруари 2016 г.
http://ec.europa.eu/dgs/health_food-safety/dyna/enews/enews.cfm?al_id=1657